諾貝爾醫學獎揭曉
2018-10-02 20:08?出處 綜合
諾貝爾醫學獎揭曉:2018年10月1日,2018諾貝爾生理學或醫學獎重磅揭曉,免疫療法先驅James P.Allison教授與Tasuku Honjo教授獲獎,表彰兩位科學家在癌癥免疫治療領域的奠定性工作。

獲獎者:James P.Allison和Tasuku Honjo,獲獎原因:發現免疫檢查點抑制癌癥療法
這兩位令人尊敬的醫學家在癌癥免疫治療領域取得了了不起的創新性成果,徹底改變了人類對抗癌癥的格局。當下,可以負責任的說,免疫療法或許會成為人類癌癥治療的新希望。
James P.Allison教授是癌癥免疫療法的先驅之一,也被稱“CTLA-4抗體Yervoy之父”。作為現代腫瘤免疫治療的奠基人之一,在研究T細胞反應的調節和癌癥免疫治療策略有著杰出貢獻,確定了T細胞受體結構,證實CTLA-4通過對抗 CD28介導的共同刺激抑制T細胞活化。
Tasuku Honjo教授是來自日本的醫學家、美國國家科學院外籍院士。1992年,Tasuku Honjo發現T細胞抑制受體PD-1,2013年依此開創了癌癥免疫療法,功績名列《Science》年度十大科學突破之首。Tasuku Honjo是德國醫學最高獎羅伯·柯霍獎的“科霍獎”得主。
抗癌的心路歷程
19世紀末,美籍醫生Coley意外的發現,手術后感染釀膿鏈球菌病人的癌癥出現了緩解跡象,第一次打開了免疫療法治療癌癥的大門。
20世紀60年代,澳籍免疫學家Burnet提出的“免疫監視理論”。
盡管免疫療法治療癌癥在理論上被實現,但如何激活T細胞(可以理解為攻擊細菌/癌細胞的“大炮”)來對抗癌癥,成為科學家們關注的一個重要的難題。
1987年,法國醫學家科學團隊發現了T細胞上的一個跨膜受體CTLA 4。
1992年,京都大學免疫學家Tasuku Honjo 本庶佑教授發現了另外一位于T細胞上的重要免疫抑制受體分子PD 1(programmed death 1)。然而,真正將PD 1和免疫聯系起來已是7年后了,這要歸功于耶魯大學陳列平教授了。他們發現腫瘤細胞表面的配體分子PD L1會通過和PD 1相結合,從而抑制T細胞激活從而發揮作用,這對于后面使用PD 1免疫療法治療癌癥,提供了重要的實驗基礎。

1996年,Jim Allison在小鼠實驗中首次發現,CTLA 4扮演的就是“剎車”的角色,抑制CTLA 4能夠激活T細胞持續的對癌癥進行攻擊。
通過不斷的人體研究,CTLA-4抗體始終表現出色,為廣大癌癥患者帶去了希望。
2011年,CTLA-4抗體制成的藥物ipilimumab (Yervoy)經過FDA批準上市,用來治療轉移性黑色素瘤,這是免疫療法的一次里程碑式的勝利。
《科學》雜志將腫瘤免疫治療列為2013 年十大科學突破的首位,免疫治療有望成為繼手術、化療、放療、腫瘤靶向治療后的新一代的腫瘤治療手段。腫瘤免疫治療包括免疫檢查點抑制劑(抗PD-1 單抗等)、治療性疫苗、CAR-T 細胞治療等。
2014年,PD 1抗體Pembrolizumab(Keytruda)通過FDA批準上市,除了在黑色素瘤上的出色表現,也其他實體瘤的治療效果,讓眾多的科學家們看到了治愈癌癥的希望。
2015年《新英格蘭醫學雜志》報道了一位49歲的黑色素瘤患者在CTLA 4抗體和PD 1抗體的聯合使用3周后,轉移瘤出現消失。這不僅僅大大增強了科學家們通過免疫療法戰勝癌癥的信心,也表明CTLA 4和PD 1通過協同作用,聯合抗癌。
2017年,美國賓夕法尼亞大學基于CAR-T療法提出的CTL019通過FDA批準上市。

國內單抗市場
PD-1 單抗已經成為抗腫瘤藥市場的超級明星,也是腫瘤免疫療法中的一顆閃耀新星!Opdivo 和Keytruda 自2014年上市以來,僅3個完整年度,2017年合計銷售額已達87.57 億美元。根據Evaluate Pharma 預測,2022 年,Opdivo 和Keytruda 合計收入有望超過194 億美元,2017-2022 復合增長率高達17%,是市場潛力最大的抗腫瘤靶向藥。
我國腫瘤年新增患者約429.16 萬人,其中約202.69 萬人可以適用于抗PD-1 單抗,約占總發病人數的47.23%。根據CA CANCER J CLIN 最新流行病學研究,我國每年新增腫瘤患者數量約429.16 萬人。根據目前全球上市兩款抗PD-1 單抗藥已獲批適應癥分析,我國每年新增腫瘤患者中約202.69 萬人適用于抗PD-1 單抗(紅色),占總發病人數的47.23%。未來,隨著抗PD-1 單抗以及聯合用藥的不斷開發,更多的新適應癥有望陸續獲批,適用患者有望進一步增加。
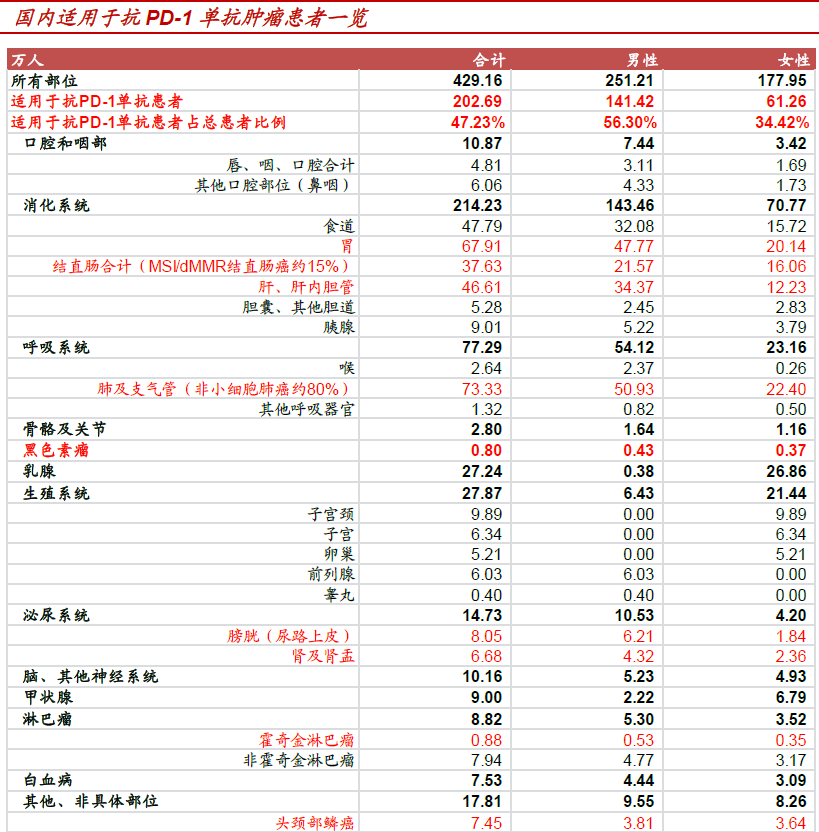
2018年是國內抗PD-1 單抗上市元年,國產產品和進口產品上市時間差距不大,國內企業有望占據主要市場!國內目前進度最快的抗PD-1 單抗是百時美施貴寶的Opdivo,已于2017 年11 月2 日向CDE提交上市申請,并進入優先審評,有望于2018 年獲批上市;默沙東的Keytruda 國內上市申請也于2018 年2 月11 日獲得CFDA 受理。
國產品種中,君實生物抗PD-1 單抗上市申請于2018 年3 月獲得CFDA 受理,恒瑞醫藥、百濟神州、信達生物有望快速跟進。根據臨床進度和遞交上市申請時間,預計包括君實生物、恒瑞醫藥、百濟神州和信達生物在內的國產抗PD-1 單抗和進口品種僅相差4-6個月,未來獲批上市時間也將差距不大。
國內在研PD-1單抗一覽
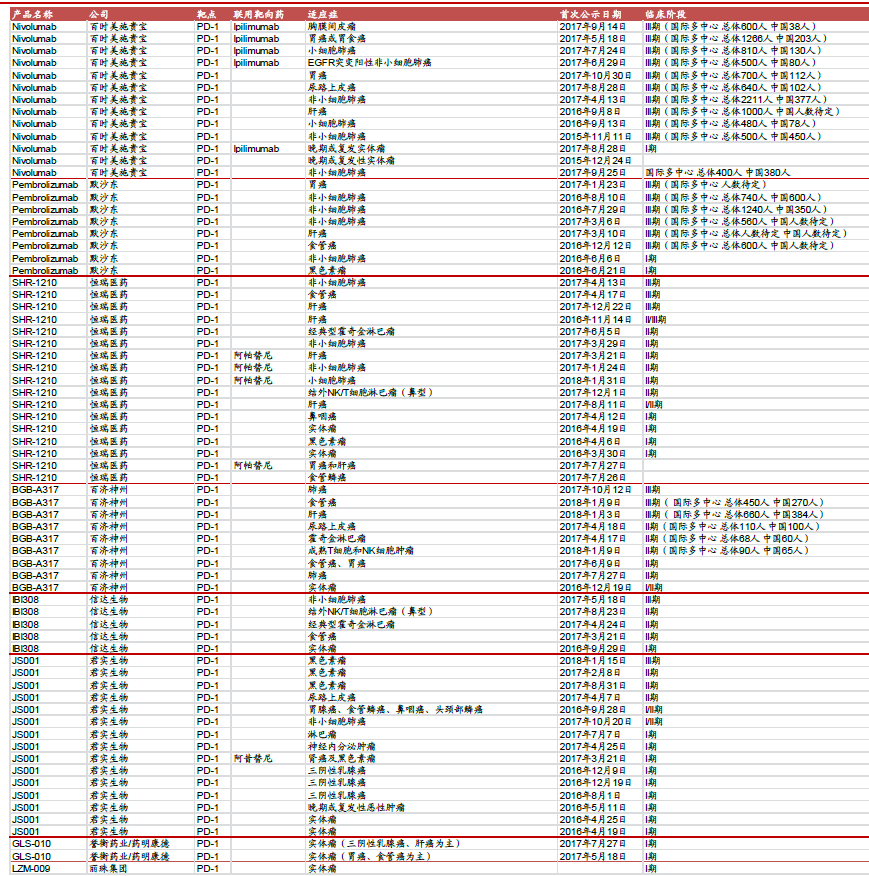
重點公司
恒瑞醫藥:重磅品種帶動業績增速加快,由國內創新走向國際創新。 公司重磅創新藥吡咯替尼和抗PD-1 單抗有望于18年陸續獲批上市。
復星醫藥:是為數不多的同時擁有抗PD-1 單抗和抗PD-L1 單抗的企業。
百濟神州:抗PD-1 單抗開展全球多中心III 期臨床,海外授權新基公司。公司抗PD-1 單抗海外授權新基,已經啟動肝癌和食管癌全球多中心III 期臨床試驗和肺癌國內III 期臨床試驗,是海外進展最快的國產抗PD-1 單抗。
君實生物:公司抗PD-1 單抗JS001 上市申請獲得受理,并同時開發多種適應癥。公司布局眾多廣譜抗腫瘤品種,未來有望形成組合用藥。
麗珠集團:抗PD-1 單抗國內外獲批臨床,加速向創新藥企業轉型。公司現金充裕,存在外延并購預期,同時向創新藥企業轉型速度加速。
本文“”來源:http://www.hangqichache.cn/news/world/71458.html,轉載必須保留網址。作者:yujeu
- 熱門內容
- 網友熱議
- 精彩內容

 西班牙左翼人士要求
西班牙左翼人士要求 美國共和黨發起罷免
美國共和黨發起罷免 美國稱危地馬拉外交
美國稱危地馬拉外交 美國議員菲利普斯將
美國議員菲利普斯將 英國小偷挑戰賽 參加
英國小偷挑戰賽 參加 石柏魁“撼”故宮 故
石柏魁“撼”故宮 故 拉里薩-里克爾梅Lar
拉里薩-里克爾梅Lar 克里米亞的前世今生
克里米亞的前世今生 阿麗娜·卡巴耶娃和普
阿麗娜·卡巴耶娃和普 釣魚島嶼最新事件中
釣魚島嶼最新事件中